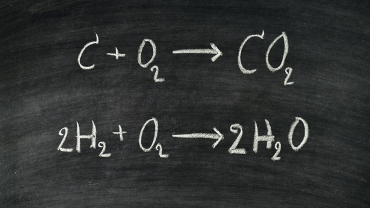Άτομα, Μόρια και Χημικές Αντιδράσεις
Η ύλη αποτελείται από μίγματα και καθαρές ουσίες. Οι καθαρές ουσίες, μπορεί να είναι χημικές ενώσεις ή χημικά στοιχεία χαρακτηρίζονται από καθορισμένες φυσικές σταθερές. Οι χημικές ενώσεις σχηματίζονται από την ένωση δύο ή περισσότερων χημικών στοιχείων με σταθερή αναλογία μαζών για κάθε ένωση. Για τη διάσπαση μίας ένωσης δεν αρκούν οι φυσικές μέθοδοι, αλλά χρειάζονται χημικές μέθοδοι όπως η ηλεκτρόλυση με την οποία η χημική ένωση νερό διασπάται στα χημικά στοιχείς υδρογόνο και οξυγόνο.
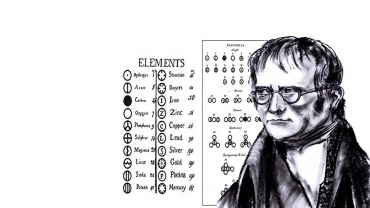
Τα άτομα ενός στοιχείου δεν είναι ορατά με γυμνό μάτι, είναι άχρωμα και έχουν την ίδια μάζα, που είναι διαφορετική από αυτή ατόμων άλλων στοιχείων. Τα άτομα ενώνονται μεταξύ τους και σχηματίζουν ενώσεις, από τις οποίες αποτελούνται όλα όσα υπάρχουν γύρω μας. Κάθε χημικό στοιχείο έχει ένα όνομα και ένα σύμβολο.
Το άτομο δεν αποτελεί το μικρότερο συστατικό της ύλης, καθώς αποτελείται και αυτό από μικρότερα σωματίδια, τα οποία ονόμασαν υποατομικά σωματίδια. Αυτά είναι τα πρωτόνια και τα νετρόνια, που βρίσκονται στο κέντρο του ατόμου και αποτελούν τον πυρήνα του ατόμου, και τα ηλεκτρόνια τα οποία περιστρέφονται γύρω από αυτόν με τη μορφή νέφους. Τα ηλεκτρόνια έχουν αρνητικό φορτίο και τα πρωτόνια θετικό, ενώ τα νετρόνια δεν έχουν φορτίο. Τα άτομα είναι ηλεκτρικά ουδέτερα και ο αριθμός των πρωτονίων σε κάθε άτομο είναι ίσος με αυτό των ηλεκτρονίων. Από τα ουδέτερα άτομα με πρόσληψη ή αποβολή ηλεκτρονίων προκύπτουν τα φορτισμένα άτομα που καλούνται ιόντα και συγκεκριμένα τα ανιόντα κατά την πρόσληψη ηλεκτρονίων και τα κατιόντα κατά την αποβολή ηλεκτρονίων. Ο ατομικός αριθμός συμβολίζει τον αριθμό των πρωτονίων ενός ατόμου και ο μαζικός το άθροισμα των πρωτονίων και των νετρονίων.
Τα άτομα ενώνονται μεταξύ τους και σχηματίζουν τα μόρια. Κάποιες ενώσεις αποτελούνται από ιόντα, ενώ τα μέταλλα σχηματίζουν πλέγματα με μεταλλικούς δεσμούς. Σε μία χημική ένωση το είδος και η αναλογία των ατόμων παραμένει πάντα σταθερό. Για τον συμβολισμό τους χρησιμοποιούνται οι χημικοί τύποι που περιγράφουν το είδος και τον αριθμό των ατόμων της ένωσης.
Στα χημικά φαινόμενα όταν πραγματοποιείται μία χημική αντίδραση, οι ουσίες που αντιδρούν μετατρέπονται σε κάποια άλλη ένωση και προκύπτει ως προϊόν μια ή περισσότερες νέες χημικές ενώσεις που έχουν νέες ιδιότητες. Στις χημικές αντιδράσεις η μάζα των προϊόντων είναι πάντα ίση με αυτή των αντιδρώντων. Μία αντίδραση για να πραγματοποιηθεί μπορεί να χρειάζεται θερμότητα, να είναι δηλαδή ενδόθερμη ή μπορεί να παράγει θερμότητα και να είναι εξώθερμη. Κατά την πραγματοποίηση μίας χημικής αντίδρασης αλλάζουν τα μόρια και οι ενώσεις που αντιδρούν και όχι τα άτομα από τα οποία αποτελούνται. Ο αριθμός και το είδος των ατόμων παραμένουν αμετάβλητα καθ' όλη τη διάρκεια της αντίδρασης.
Κάθε χημική αντίδραση περιγράφεται από μια χημική εξίσωση, στην οποία φαίνονται ποια μόρια αντέδρασαν, τι προϊόντα παράχθηκαν, οι αναλογίες αυτών καθώς και η φυσική τους κατάσταση.