Η εξουδετέρωση
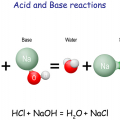
Είναι γνωστό ότι όταν μια βάση όπως το υδροξείδιο του νατρίου (NaOH) διαλυθεί σε νερό ελευθερώνει ανιόντα υδροξειδίου, ΟΗ-, τα οποία καθιστούν το διάλυμα βασικό ή αλκαλικό με pH > 7. Αντίστοιχα, κατά τη διάλυση ενός οξέος όπως το υδροχλωρικό HCl στο νερό δημιουργούνται κατιόντα υδρογόνου, H +, τα οποία καθιστούν το διάλυμα όξινο με pH < 7. Άρα όταν σε διάλυμα οξέος προστεθεί διάλυμα βάσης, τότε στην ουσία γίνεται προσθήκη ιόντων υδροξειδίου, ΟΗ-, τα οποία αντιδρούν με τα κατιόντα υδρογόνου και δίνουν νερό (H2O).
H χημική αυτή αντίδραση μεταξύ των κατιόντων υδρογόνου, Η+, που προέρχονται από το οξύ και των ανιόντων υδροξειδίου, ΟΗ - , που προέρχονται από τη βάση κατά την οποία σχηματίζονται μόρια νερού λέγεται εξουδετέρωση και παριστάνεται ως εξής:
Η+(aq) + ΟΗ-(aq) → Η2O(l)
Καθώς συνεχίζεται η προσθήκη του διαλύματος της βάσης στο όξινο διάλυμα, εξουδετερώνονται όλο και περισσότερα κατιόντα υδρογόνου (Η+) πράγμα που συνεπάγεται αύξηση της τιμής του pH του όξινου διαλύματος. Τη χρονική στιγμή που θα δεσμευτούν όλα τα κατιόντα υδρογόνου (Η+) από ίσο αριθμό ανιόντων υδροξειδίου (ΟΗ-) η εξουδετέρωση είναι πλήρης και το διάλυμα που προκύπτει είναι ουδέτερο. Προκύπτει δηλαδή διάλυμα που δεν έχει ούτε όξινες ούτε βασικές ιδιότητες και το pH του είναι ίσο με 7 όπως και του καθαρού νερού.
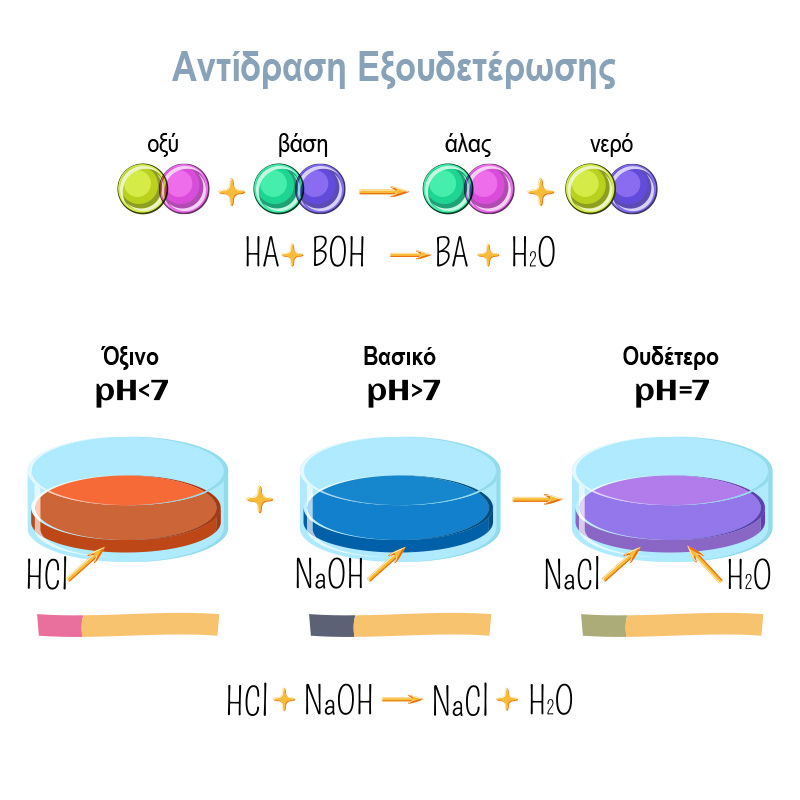
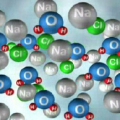
Στο σημείο αυτό πρέπει να αναφερθεί ότι σύμφωνα με την εξίσωση της χημικής αντίδρασης δημιουργείται στα παραπάνω υδατικά διαλύματα, εκτός από το νερό (από τα ιόντα υδρογόνου και υδροξειδίου), και ένα άλας. Το άλας που δημιουργείται από την εξουδετέρωση υδροχλωρικού οξέος με καυστικό νάτριο, είναι το χλωριούχο νάτριο (NaCl) το οποίο είναι ευδιάλυτο στο νερό. Έτσι το τελικό διάλυμα περιέχει "διαλυμένο άλας", δηλαδή κατιόντα νατρίου (Νa+) και ανιόντα χλωρίου (Cl-). Το τελικό διάλυμα δε θα διαφέρει σε τίποτα από ένα διάλυμα που θα παρασκευάζαμε διαλύοντας μια ποσότητα καθαρού μαγειρικού άλατος σε νερό.
Οξύ + Βάση → Άλας + Νερό
Αν αφήσουμε το δοχείο μετά την αντίδραση στον πάγκο του εργαστηρίου ή αν το θερμάνουμε για να επιταχύνουμε την εξάτμιση του νερού, θα απομείνει τελικά ένα άσπρο στερεό υπόλειμμα, που δεν είναι τίποτα άλλο από μαγειρικό αλάτι. Αν με το pHμετρικό χαρτί επιβεβαιώσουμε ότι το διάλυμά μας ήταν πράγματι ουδέτερο μετά το τέλος της αντίδρασης, τότε μπορούμε να γευτούμε το στερεό υπόλειμμα και θα διαπιστώσουμε ότι είναι αλμυρό. (Θα μπορούσαμε κάλλιστα να το βάλουμε στη σαλάτα μας !)