Ατομικός και μαζικός αριθμός
Κάθε άτομο ενός στοιχείου χαρακτηρίζεται από δύο αριθμούς. Τον ατομικό αριθμό, Ζ, και τον μαζικό αριθμό, Α.
Ο ατομικός αριθμός, Ζ, δηλώνει τον αριθμό των πρωτονίων που υπάρχουν σε ένα άτομο. Για παράδειγμα το κάλιο, K, που έχει 19 πρωτόνια στον πυρήνα του έχει Ζ ίσο με 19. Ο ατομικός αριθμός είναι χαρακτηριστικός για το κάθε στοιχείο και καθορίζει τις χημικές του ιδιότητες.
Ο μαζικός αριθμός, Α, δηλώνει το άθροισμα του πλήθους των πρωτονίων και των νετρονίων του ατόμου. Ισχύει λοιπόν A = Z + N.
Το πλήθος των νετρονίων δεν είναι πάντα ίσο με αυτό των πρωτονίων. Συνήθως, ο αριθμός των νετρονίων στον πυρήνα ενός ατόμου είναι μεγαλύτερος από τον αριθμό των πρωτονίων.
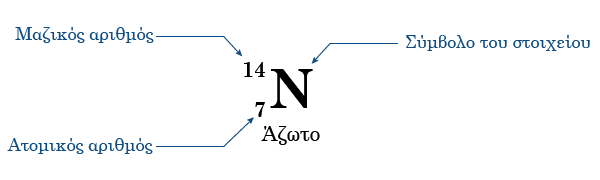
Για να χαρακτηριστεί πλήρως ο πυρήνας ενός ατόμου αναγράφεται στα αριστερά του συμβόλου του στοιχείου, κάτω ο ατομικός αριθμός και πάνω ο μαζικός αριθμός. Το άζωτο, που έχει Α=7 και Ζ=14 συμβολίζεται ως 147N.
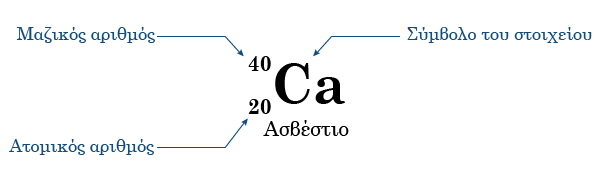
Αντιστοίχως, το ασβέστιο Ca που έχει Α=40 και Ζ=20 συμβολίζεται ως 4020Β:
Για την απλούστευση των χημικών συμβολισμών, όταν μας ενδιαφέρει κυρίως το άτομο - στοιχείο και όχι η δομή του πυρήνα του, χρησιμοποιείται απλώς το σύμβολο του στοιχείου χωρίς τους αριθμούς.