Ορισμός των βάσεων κατά Arrhenius
O Σουηδός χημικός, Svante Αrrhenius, όπως και στην περίπτωση των οξέων αναζήτησε την αιτία της εμφάνισης των κοινών ιδιοτήτων των βάσεων στη δομή τους. Παρατήρησε λοιπόν, ότι έχουν στο μόριο τους μια κοινή ομάδα το υδροξύλιο (ΟΗ), που δεν υπάρχει στα οξέα. Με βάση τη διαπίστωση αυτή και γνωρίζοντας ότι το νερό μπορεί να διαλύσει πολλές χημικές ενώσεις, με αποτέλεσμα τη διάσταση τους σε ιόντα, ο Αrrhenius πρότεινε ότι:
Βάση είναι κάθε χημική ένωση η οποία, όταν διαλύεται στο νερό, ελευθερώνει ανιόντα υδροξειδίου, ΟΗ-, στο διάλυμα.
Επιπλέον, σύμφωνα με τον Arrhenius όσο περισσότερα είναι τα ανιόντα υδροξυλίου (ΟΗ-) στο διάλυμα, τόσο πιο βασικό ή αλκαλικό είναι.
Είναι σημαντικό να τονιστεί ότι (όπως γνωρίζουμε σήμερα) η ύπαρξη της ομάδας του υδροξυλίου (ΟΗ) σε μια χημική ένωση δε συνεπάγεται απαραίτητα ότι η ένωση αυτή αποτελεί βάση. Για να χαρακτηριστεί μια ένωση βάση πρέπει κατά τη διάλυση της στο νερό να ελευθερώνει ή να δημιουργεί τα ανιόντα υδροξειδίου (ΟΗ-). Για παράδειγμα, ενώ η αιθανόλη (CH3CH2OH) περιέχει στο μόριο της OH, δεν παρουσιάζει βασικό χαρακτήρα. Επιπλέον, δεν είναι απαραίτητο μια ένωση να έχει στο μόριό της την υδροξυλική ομάδα για να έχει ένα υδατικό διάλυμά της βασικό χαρακτήρα.
Μπορεί κατά τη διάλυση της στο νερό να αντιδρά με αυτό και έτσι να παράγονται τα ανιόντα υδροξειδίου (ΟΗ-). Σε αυτή την κατηγορία ανήκει η αμμωνία. Αυτές ήταν κάποιες από τις αδυναμίες της θεωρίας του Αrrhenius, γι΄αυτό και διατυπώθηκαν αργότερα πιο ολοκληρωμένες θεωρίες σχετικές με τις βάσεις που συμπεριέλαβαν και άλλες ενώσεις.
Αυτά είναι κάποια παραδείγματα διάστασης βάσεων στο νερό:
Υδροξείδιο του νατρίου:
NaOH(aq) → Na+(aq) + OH-(aq)
Υδροξείδιο του καλίου:
KOH(aq) → K+(aq) + OH-(aq)
Υδροξείδιο του ασβεστίου:
Ca(OH)2(aq) → Ca2+(aq) + 2OH-(aq)
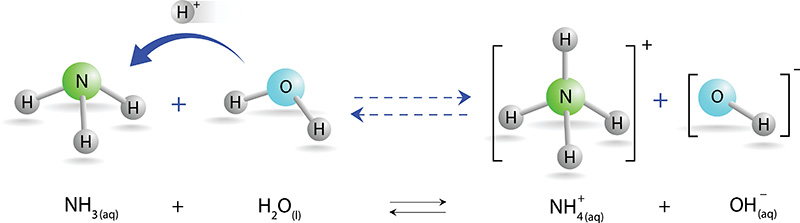
Αμμωνία:
Η αμμωνία (NH3) κατά τη διάλυση της στο νερό αποσπά ένα πρωτόνιο (Η+) από ένα μόριο νερού (Η2Ο) και ενώνεται με αυτό δημιουργώντας το θετικό ιόν (κατιόν) του αμμωνίου, (ΝΗ4+). Από το μόριο του νερού απομένει το αρνητικό ιόν (ανιόν) του υδροξειδίου,( ΟΗ-), στο οποίο οφείλονται οι βασικές ή αλκαλικές ιδιότητες του διαλύματος.
NH3(g) + H2O(l) ⇄ NH4+(aq) + OH-(aq)