Τα ιόντα
Είναι γνωστό ότι τα άτομα είναι ηλεκτρικά ουδέτερα καθώς έχουν ίσο αριθμό θετικά φορτισμένων πρωτονίων και αρνητικά φορτισμένων ηλεκτρονίων. Παρόλα αυτά είναι δυνατό να απομακρυνθεί από ένα άτομο ή να προστεθεί σε ένα άτομο ένα ή περισσότερα ηλεκτρόνια.
Η προσθήκη ή απομάκρυνση ηλεκτρονίων σε ένα αρχικώς ουδέτερο άτομο με ίσο αριθμό ηλεκτρονίων και πρωτονίων, έχει σαν αποτέλεσμα το πλήθος των ηλεκτρονίων να καθίσταται μεγαλύτερο ή μικρότερο από αυτό των πρωτονίων και έτσι το άτομο θα αποκτήσει αντιστοίχως αρνητικό ή θετικό φορτίο. Πολλά άτομα στοιχείων έχουν την τάση να αποβάλλουν ή προσλαμβάνουν ηλεκτρόνια σχετικά εύκολα και δίνουν ιόντα. Τα φορτισμένα αυτά άτομα καλούνται ιόντα και μπορεί να έχουν θετικό ή αρνητικό φορτίο
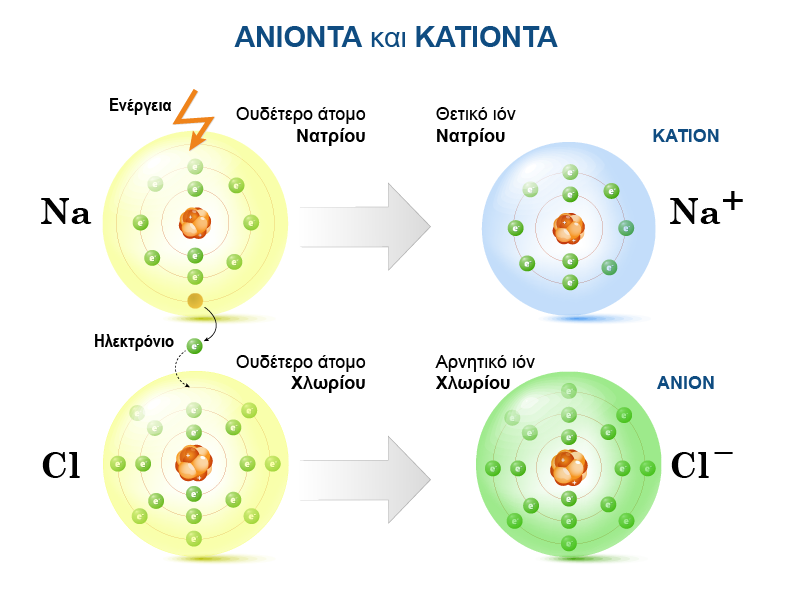
Ένα θετικά φορτισμένο ιόν ονομάζεται κατιόν. Τα άτομα του νατρίου Νa έχουν ατομικό αριθμό 11 και είναι όπως όλα τα άτομα ηλεκτρικά ουδέτερα, αλλά μπορούν εύκολα να αποβάλουν ένα ηλεκτρόνιο. Καθώς μετά την απομάκρυνση του ηλεκτρονίου τα άτομα έχουν ένα παραπάνω πρωτόνιο απ’ ότι ηλεκτρόνια, μετατρέπονται σε θετικά φορτισμένα ιόντα με ένα στοιχειώδες θετικό φορτίο, δηλαδή σε κατιόντα. Για τον συμβολισμό ενός κατιόντος τοποθετείται δεξιά από το σύμβολο του στοιχείου του ως εκθέτης ο αριθμός των στοιχειωδών θετικών φορτίων και ένα +. Εάν το κατιόν έχει ένα στοιχειώδες φορτίο ο αριθμός 1 παραλείπεται. Έτσι, το κατιόν του νατρίου συμβολίζεται ως Νa +, ενώ το κατιόν του ασβεστίου ως Ca2+.
Ένα αρνητικά φορτισμένο ιόν ονομάζεται ανιόν. Τα άτομα του χλωρίου Cl έχουν ατομικό αριθμό 17 και είναι και αυτά ηλεκτρικά ουδέτερα. Μπορούν όμως με σχετική ευκολία να προσλάβουν ένα ηλεκτρόνιο και να μετατραπούν σε ανιόντα. Καθίστανται λοιπόν θετικά φορτισμένα ιόντα με ένα στοιχειώδες αρνητικό φορτίο, αφού έχουν ένα ηλεκτρόνιο περισσότερο απ’ ότι πρωτόνια. Για τον συμβολισμό ενός ανιόντος όπως και στα κατιόντα, γράφεται δεξιά από το σύμβολο του στοιχείου του ως εκθέτης ο αριθμός των στοιχειωδών αρνητικών φορτίων και ένα - . Εάν το ανιόν έχει ένα στοιχειώδες φορτίο ο αριθμός 1 παραλείπεται. Έτσι, το ανιόν του χλωρίου, συμβολίζεται ως Cl -.
Είναι σημαντικό να τονιστεί, ότι για να σχηματιστεί ένα ανιόν ή ένα κατιόν χρειάζονται δυο άτομα, καθώς πρέπει από το ένα άτομο να απομακρυνθούν ηλεκτρόνια τα οποία θα προσληφθούν από το άλλο. Τα ηλεκτρόνια δεν κυκλοφορούν ελεύθερα στη φύση αλλά μετακινούνται μόνο από άτομο σε άτομο.