Η όξινη βροχή
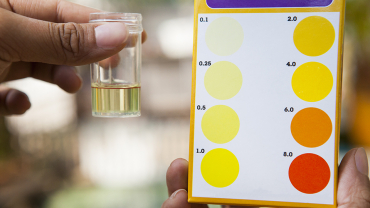
Το νερό της βροχής είναι ελαφρώς όξινο. Το pΗ της είναι γύρω στο 5.6 που οφείλεται στον μερικό ιοντισμό του ανθρακικού οξέος (H2CO3), που δημιουργείται λόγω της διάλυσης του διοξειδίου του άνθρακα (CO2) του ατμοσφαιρικού αέρα στο νερό της βροχής κατά την αντίδραση:
CO2(g) + H2O(l) → H2CO3(aq) → Η+(aq) + HCO3-(aq)
Η όξινη βροχή όμως έχει μέχρι και 25 φορές μεγαλύτερη οξύτητα από τη φυσιολογική. Αυτό οφείλεται στην παρουσία πολύ ισχυρών οξέων. Στις βιομηχανικές και στις αστικές περιοχές η περιεκτικότητα της ατμόσφαιρας σε οξείδια - ρύπους είναι ιδιαίτερα υψηλή. Η καύση των ορυκτών καυσίμων, υγραέριο, πετρέλαιο, άνθρακας κ.ά. από:
- τις μηχανές εσωτερικής καύσης, όπως οι κινητήρες των αυτοκινήτων, αεροπλάνων κ.α.
- τους καυστήρες, π.χ. κεντρικής θέρμανσης ή παραγωγής ατμού μεγάλων κτιρίων και βιομηχανικών εγκαταστάσεων
παράγει οξείδια του άνθρακα (CO και CO2), του θείου (SO2 και SO3) και του αζώτου (ΝΟ και NO2).

Το SO2 αντιδρά αργά με το O2 του αέρα παράγοντας SO3 και στη συνέχεια αυτό διαλύεται στο το νερό της βροχής με αποτέλεσμα το σχηματισμό του ισχυρού θειικού οξέος (Η2SO4).
2SO2(g) + O2(g) → 2SO3(l)
SO3(l) + Η2Ο(l) —› Η2SO4(aq)
To ΝO αντιδρά επίσης με το O2 του αέρα και στη συνέχεια με το νερό της βροχής με αποτέλεσμα το σχηματισμό του ισχυρού νιτρικού οξέος (HNO3) και του ασθενούς νιτρώδους οξέος (HNO2).
2NO(g) + O2(g) → 2NO2(g)
2NO2(g) + Η2Ο(l) → HNO3(aq) + HNO2(aq)
Τα οξέα αυτά διαλύονται στο νερό της βροχής μετατρέποντας την σε όξινη με pΗ από 3,5 έως 4,5. Αυτά αποτίθενται ακόμα στο έδαφος και στις λίμνες. Έτσι, ένας καλύτερος όρος για την όξινη βροχή είναι "όξινη απόθεση" ή "όξινα μετεωρικά κατακρημνίσματα".