Τα άλατα
Τα άλατα είναι ενώσεις που προέρχονται από την εξουδετέρωση των οξέων με τις βάσεις. Χρησιμοποιείται η λέξη "εξουδετέρωση" επειδή κατά την αντίδραση ενός οξέος με μια βάση, καταστρέφονται ή αλλιώς εξουδετερώνονται τόσο οι ιδιότητες της βάσης όσο και του οξέος.
Οξύ + Βάση → Άλας + Νερό
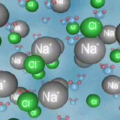
Αντιπροσωπευτικό παράδειγμα είναι η εξουδετέρωση διαλύματος υδροξειδίου του νατρίου από διάλυμα υδροχλωρικού οξέος, όπου εκτός από νερό (Η2Ο) που προέρχεται από την αντίδραση ιόντων Η+ και ΟΗ- προκύπτει και το άλας χλωριούχο νάτριο (ΝaCl) που προέρχεται από την αντίδραση των ιόντων Νa + και Cl -. Οι ιοντικές αντιδράσεις κατα την εξουδετέρωση του υδροχλωρικού οξέος με το υδροξείδιο του νατρίου είναι:
Η+(aq) + ΟΗ-(aq) → Η2O(l) και Νa+(aq) + Cl-(aq)→ NαCl(aq)
Το NaCl που παρασκευάζεται είναι ευδιάλυτο άλας γι' αυτό και παραμένει διαλυμένο στο νερό. Το νερό έχει την ικανότητα να κρατάει σε απόσταση (διάσταση) τα ιόντα Na+ και Cl- μέσα στη μάζα του. Αν εξατμιστεί το νερό θα προκύψει το λευκό, κρυσταλλικό, στερεό άλας NaCl που είναι το κοινό μαγειρικό αλάτι.
Εκτός όμως από τα ευδιάλυτα άλατα κατά την εξουδετέρωση ενός οξέος από μια βάση μπορεί να προκύψουν και δυσδιάλυτα άλατα στο νερό. Για παράδειγμα, κατά την εξουδετέρωση του θειικού οξέος (H2SO4) από υδροξείδιο του ασβεστίου (Ca(OH)2) προκύπτει το δυσδιάλυτο άλας του θειικού ασβεστίου (CaSO4) το οποίο καταβυθίζεται ως στερεό και είναι ο γνωστός γύψος. Οι ιοντικές αντιδράσεις που λαμβάνουν χώρα κατά την εξουδετέρωση του θειικού οξέος από υδροξείδιο του ασβεστίου είναι:
2Η+(aq) + 2ΟΗ-(aq) → 2Η2O(l)
και Ca2+(aq) + SO42-(aq) → CaSO4(aq) ↓ (καταβυθίζεται ως λευκό ίζημα)
Γενικά οι κοινές ιδιότητες των αλάτων είναι οι εξής:
| Ιδιότητες αλάτων | |
|---|---|
| 1 | Είναι στερεές κρυσταλλικές ουσίες. |
| 2 | Προέρχονται συνήθως από την εξουδετέρωση των οξέων από τις βάσεις. |
| 3 | Έχουν υψηλά σημεία ζέσεως και τήξεως. |