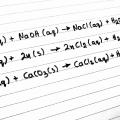Ευδιάλυτα και δυσδιάλυτα άλατα
Τα άλατα, ανάλογα με τη διαλυτότητά τους στο νερό διακρίνονται σε ευδιάλυτα και δυσδιάλυτα.
Παράδειγμα ευδιάλυτου άλατος στο νερό είναι το χλωριούχο νάτριο που παρασκευάζεται από την ανάμειξη διαλυμάτων υδροχλωρικού οξέος και καυστικού νατρίου, δηλαδή την εξουδετέρωση τους.
Από την άλλη μεριά κατά την ανάμιξη ανθρακικού οξέος (H2CO3) και υδροξειδίου του ασβεστίου (Ca(OH)2) σχηματίζεται το δυσδιάλυτο άλας ανθρακικό ασβέστιο (CaCO3), το οποίο καταβυθίζεται στον πυθμένα του δοχείου ως λευκό στερεό ίζημα.
Γενικά ως διαλυτότητα μιας ουσίας, ορίζεται η μέγιστη δυνατή ποσότητα της ουσίας που μπορεί σε ορισμένη θερμοκρασία να διαλυθεί σε ορισμένη ποσότητα διαλύτη. Ο συνηθέστερος διαλύτης είναι το νερό. Η διαλυτότητα εκφράζεται ως η ποσότητα σε γραμμάρια (g) του άλατος που μπορούν να διαλυθούν σε 100 γραμμάρια (100 g) νερού στους 25 ο C.
Οι διαλυτότητες μερικών από τα σπουδαιότερα άλατα δίνονται στο πίνακα που ακολουθεί:
| Άλας | Χημικός τύπος | Διαλυτότητα (g άλατος / 100 g νερού) |
|---|---|---|
| Χλωριούχο νάτριο | NaCl | 36 |
| Βρωμιούχο νάτριο | NaBr | 95 |
| Ιωδιούχο νάτριο | NaI | 185 |
| Ιωδιούχο κάλιο | KI | 148 |
| Νιτρικός άργυρος | AgNO3 | 245 |
| Ανθρακικό ασβέστιο | CaCO3 | Σε ίχνη διαλυτό (0,0013) |
| Θειικό ασβέστιο | CaSO4 | Δυσδιάλυτο (0,21) |
| Χλωριούχος άργυρος | AgCl | Αδιάλυτο (0,0000001) |
| Φωσφορικό ασβέστιο | Ca3(PO4)2 | Δυσδιάλυτο (0,002) |